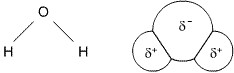|
Wasser ist die Verbindung von einem Sauerstoffatom mit zwei Wasserstoffatomen: H2O. Wasser macht etwa 70% des Zellgewichtes aus. Die meisten biochemischen Reaktionen finden in einem wässerigen Milieu statt.
Das Sauerstoffatom zieht Elektronen teilweise von den Kernen der Wasserstoffatome weg. Dadurch entsteht ein leicht positiver Bereich bei den Wasserstoffatomen und ein schwach negativer Bereich beim Sauerstoffatom. Durch diese asymmetrische Verteilung der Elektronen wird das Wassermolekül polar (die Nettoladung ist jedoch weiterhin neutral).
Abb. 1: Das Wassermolekül und seine Ladungsverteilung.
Abb. 2: Wasserstoff-Bindung: wegen der leichten negativen Ladung im Bereich des Sauerstoffatoms und der leichten positiven Ladung im Bereich der Wasserstoffatomen können sich sogenannte Wasserstoff-Bindungen ausbilden. Aufgrund ihrer Polarisation können zwei benachbarte Wassermoleküle eine Bindung ausbilden, die als Wasserstoff-Bindung bezeichnet. Diese Bindung ist zwar nur schwach (sie beträgt lediglich 1/20 der Stärke einer kovalenten Bindung), spielt aber in der Biochemie eine grosse Rolle. Wassermoleküle verbinden sich daher zu einem Wasserstoff-Brücken-Netzwerk, das für viele ungewöhnliche Eigenschaften des Wassers verantwortlich ist, so z.B. für seine hohe Oberflächenspannung.
Wegen ihrer polaren Natur sammeln sich Wassermoleküle um Ionen und andere polare Moleküle. Diese Substanzen sind daher in Wasser gut löslich und werden als hydrophil ("wasserliebend") bezeichnet.
Abb. 3: Hydrophile Substanzen Nichtpolare Moleküle dagegen unterbrechen die Wasserstoffbrücken-Struktur des Wassers, sind daher in Wasser schlecht löslich und werden lipophil (oder hydrophob) genannt.
Werden zwei wässerige Lösungen unterschiedlicher Konzentration durch eine Membran voneinander getrennt, die nur Wasser, nicht aber die gelösten Teilchen, durchlässt, wird Wasser in die konzentriertere Lösung wandern. Diesen Vorgang nennt man Osmose. Die Bewegung des Wassers aus einer hypotonen Lösung in eine hypertone Lösung bewirkt eine Erhöhung des hydrostatischen Druckes auf Seite der hypertonen Lösung. Zwei Kompartimente mit unterschiedlich konzentrierten Lösungen sind durch eine semipermeable Membran getrennt. Es kommt zu einer Verschiebung von Wasser, die gelösten Teilchen bleiben in ihrem Kompartiment "gefangen". In der Biologie bedeutet dies, dass Zellen in einem hypertonen Milieu Wasser abgegeben und damit schrumpfen, Zellen in einer hypotonen Umgebung dagegen durch Wasseraufnahme anschwellen.
|
||||||||||
|
02.02.2001 /hpk |